Можно ли принимать изопринозин во время месячных
Линаск Л.И. Григорьева Е.Е.
Главной особенностью ВПЧинфекции считают ее широкое распространение среди подростков и молодых женщин преимущественно до 25 лет [3]. Низкая сексуальная культура населения,
частая смена половых партнеров, незащищенный секс, вредные привычки (курение, токсикомания, алкоголизм) увеличивают риск развития ВПЧинфекции, что способствует росту числа воспалительных заболеваний генитального тракта, нарушению репродуктивной функции, невынашиванию беременности и внутриутробного инфицирования плода, а также формированию цервикальной интраэпителиальной неоплазии шейки матки. Вместе с тем отмечено, что у подростков и молодых женщин происходит более быстрое самопроизвольное очищение (элиминация) от ВПЧ и регрессия имеющейся ВПЧассоциированной патологии по сравнению с женщинами более позднего возраста. По результатам исследований, среднее время элиминации ВПЧ у подростков составляет 8 месяцев (CDC, 1999). По наблюдениям С.И. Роговской и В.Н. Прилепской (2006), в возрасте 1825 лет этот период увеличивается до 1,52 лет у каждой второй пациентки. Локальные показатели инфицированности взаимосвязаны с другими генитальными инфекциями. трихомониазом, хламидиозом, микоуреаплазмозом, кандидозом и т.д. [7,8].
Большинство исследователей отмечают значительное разнообразие типов папилломавирусов. Чаще всего обнаруживается вирус 16 типа, следующим по частоте является вирус типа 18. На долю этих вирусов приходится около 50% от общего числа ВПЧ. Вирус папилломы человека может оказывать продуктивное (с образованием кондилом и папиллом) и непродуктивное действие на эпителий. Результатом непродуктивного действия являются внутриэпитеальные поражения, такие как цервикальная интраэпителиальная неоплазия, рак [3,11].
Наиболее уязвимым участком для воздействия вируса является зона трансформации участок замещения цилиндрического эпителия плоским. Возможно, тропность ВПЧ к клеткам, претерпевающим метаплазию, связана с их повышенной чувствительностью к вирусной инфекции [9,11], поэтому наличие эктопии и других заболеваний на фоне вирусной инфекции является отягощающим обстоятельством для развития рака шейки матки .
Многообразие типов вирусов, возможность вызывать как продуктивное, так и непродуктивное действие на эпителий, формирование различных патологических процессов на шейке матки и наружных половых органах, сочетание вирусов с другими инфекционными агентами требуют дифференцированного подхода к консервативному лечению и избирательной оценке необходимости инвазивных методик.
По мнению В.А. Головановой и соавт. (1998), высокая частота патологии шейки матки у подростков и юных женщин связана с биологической незрелостью шейки матки, небольшим промежутком времени между менархе и началом половой жизни, ранним половым дебютом, наличием более 5 половых партнеров, что может стать фактором риска развития цервикальной интраэпителиальной неоплазии. Значимыми факторами риска для возникновения папилломавирусной инфекции являются эктопия и бактериальный вагиноз.
Комплексная диагностика ВПЧинфекции применительна к патологии шейки матки, хорошо разработана и предполагает использование следующих методов: клиниковизуальный, кольпоскопия, ВПЧтест и один из морфологических методов (цитологический РАРтест или гистологическое исследование прицельно взятого биоптата шейки матки).
Несмотря на расширение диапазона методов лечения (химио, крио, лазеро, электродеструкция), которые применяются при доброкачественных заболеваниях шейки матки, не существует единых подходов к выбору метода и значимых критериев преимущества одной методики перед другой. Эффективность терапии во многом зависит от выбора метода лечения, использования иммунокорригирующей терапии и целесообразности комбинированного лечения с применением деструктивного воздействия на шейку матки. Большинство исследователей подчеркивают неудачу методов локальной деструкции, отмечают частые рецидивы ВПЧ инфекции на фоне иммунодефицита, обосновывают целесообразность иммунотерапии [2].
В.Н. Прилепская и С.И. Роговская предлагают комбинированное деструктивное лечение папилломавирусных поражений шейки матки проводить на фоне приема иммунопрепаратов, снижающих активность вируса и повышающих иммунитет. Разумная иммунокоррекция повышает эффективность терапии и снижает вероятность рецидива [3,4,7].
Наиболее широкое применение получили интерфероны и их индукторы, иммуномодуляторы. Эти препараты стимулируют неспецифический иммунитет, усиливают продукцию интерлейкинов, повышая синтез антител, стимулируют хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфноядерных клеток.
В настоящее время имеется большой выбор препаратов активаторов иммунитета. Противовирусный препарат Изопринозин (производства Тева фармацевтические предприятия Лтд. Израиль), содержит активное вещество инозин пранобекс, который подавляет репликацию ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Кроме противовирусного действия, препарат обладает и иммуномодулирующим свойством за счет комплекса инозина, что повышает его доступность для лимфоцитов.
Целью настоящего исследования явилось изучение клинической эффективности препарата Изопринозин в монотерапии и комплексном лечении заболеваний шейки матки при ВПЧинфекции у подростков и юных женщин.
Материалы и методы
Всего обследовано 74 пациентки с патологией шейки матки на фоне ВПЧинфекции в возрасте от 15 до 25 лет (средний возраст 19,40,2 лет). Всем пациенткам проведено комплексное обследование, включающее изучение анамнеза, общий и гинекологический осмотр, расширенную кольпоскопию, бактериоскопию вагинальных мазков, окрашенных по Граму, ПЦРтипирование, цитологическое исследование соскобов с шейки матки.
Всем обследованным в монотерапии или при комбинированном лечении назначался Изопринозин .
Возрастная структура обследуемых: подростки в возрасте до 18 лет 35 (47,3%), молодые женщины 1925 лет 38 (51,9%), в основном учащаяся молодежь (студентки ВУЗов и колледжей).
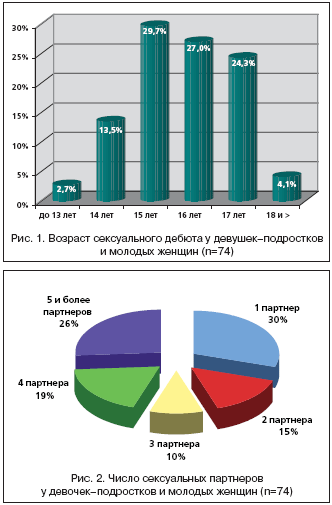
Нами проведена оценка среднего возраста начала половой жизни, количества и частоты смены половых партнеров. Анализ показал, что средний возраст начала половой жизни составил 15,90,1 лет. На рисунках 1 и 2 представлены диаграмма полового дебюта и полигамности половых связей. Только каждая третья имела постоянного полового партнера, у каждой четвертой отмечена полигамность половых связей (более 5 партнеров). У 52 (70,3%) менархе отмечено до 14 лет, у 22 (29,7%) после 14 лет, причем у каждой третьей наблюдалось позднее менархе. У большинства женщин 54 (72,9%) менструальный цикл имел регулярный характер, у каждой пятой месячные были нерегулярные (опсо или гиперполименореи).
При изучении соматического анамнеза установлено, что хронический тонзиллит и другие очаги инфекции носоглотки имели место у 21 (28,4%) пациентки, заболевания желудочнокишечного тракта у 20 (27%), вегетососудистая дистония у 25 (33,8%). Индекс соматических заболеваний составил 1,2 на 1 пациентку. Изучение анамнеза перенесенных детских инфекций показал, что каждая вторая девочкаподросток и молодая женщина переболела ветряной оспой, каждая третья коревой краснухой; респираторновирусные инфекции были у 38 (51,3%) пациенток. Высокий инфекционный индекс, составляющий более 1,5 на 1 пациентку, свидетельствует о возможных изменениях иммунного статуса.
Особый интерес представляло изучение гинекологического анамнеза, при котором установлено, что воспалительные процессы наружных и внутренних половых органов составили более 85%. Несмотря на молодой возраст обследуемых, у 5 (6,8%) имел место острый эндометрит, у 3 (4,1%) воспалительный процесс придатков матки и у 56 (75,7%) отмечался вульвовагинит. При всех эпизодах воспалительных заболеваний ранее проводилось лечение.
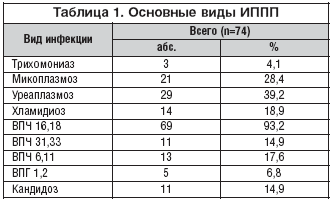
При гинекологическом осмотре в 100% выявлена патология шейки матки (эрозия, цервициты, лейкоплакии и т.д.). Определение инфекций, передаваемых половым путем, методом ПЦР и бактериоскопии, позволило установить не только различное типирование ВПЧинфекции, но и многофакторные причины воспалительных изменений на шейке матки. Моноинфекция имела место лишь у 18 (24,3%), два инфекционных фактора отмечены у 31(41,9%) пациентки, три и более инфекционных агента выявлены у 25 (33,8%) обследуемых. На одну пациентку приходится 2,4 возбудителя.
Как видно из таблицы 1, чаще всего определялся вирус папилломы человека 16,18 типа, который выявлен в 93,2%; ВПЧ 31,33 типа и ВПЧ 6,11 установлены в 14,9 и 17,6% соответственно. Следует отметить, что вирус папилломы человека, как моноинфекция, был только у каждой четвертой, у остальных 75% наиболее частыми сочетаниями являлись уреа и микоплазменные возбудители. Процент микоплазмоза составил 28,4, а уреаплазмоза 39,2. Хламидии определены у каждой пятой, трихомонады выявлены у 3 (4%), кандиды у 11 (14,9%).
Всем пациенткам до начала лечения и после него проводилась простая и расширенная кольпоскопия. На начальном этапе обследования выявлены разнообразные кольпоскопические картины: эктопия с зоной трансформации, множественными открытыми и закрытыми протоками желез, признаки очагового и диффузного кольпита, зона трансформации с атипичным эпителием в виде лейкоплакии, йоднегативные зоны, мозаика в различных сочетаниях друг с другом. При цитологическом исследовании соскобов с шейки матки I тип цитограммы установлен у 39,2% обследованных, II тип у 60,8%.
Высокий процент инфицированности, наличие цитограммы воспаления значительно повышают риск развития дисплазий. Учитывая молодой возраст пациенток, гистологическое исследование проводилось лишь по особым показаниям при осложненных формах эктопии, лейкоплакии и цитологически установленной дисплазии. Дисплазия установлена у 6 (8,1%), причем умеренно выраженная дисплазия составила 33,3%, то есть имела место у каждой третьей из шести. Также у каждой третей из всех обследованных имела место лейкоплакия. Проведенные углубленные исследования (кольпоскопическая визуализация и цитологическая диагностика) явились показанием для взятия гистологических исследований у 28 (37,8%) юных и молодых женщин. В подавляющем большинстве определена простая лейкоплакия, прогрессирующий эндоцервикоз.
Несмотря на то, что у всех пациенток выявлена ВПЧ инфекция, специфическая противовирусная терапия Изопринозином назначалась сразу только 18 пациенткам, остальным потребовались антибактериальная и санационная терапии, направленные на элиминацию возбудителей патогенной и условнопатогенной флоры. При верификации инфекции проводилась специфическая терапия основного инфекционного заболевания. При урео и микоплазмозе, хламидиозе использовались антибактериальные препараты, при кандидозе противогрибковые, при бактериальном вагинозе коррекция биоценоза по общим терапевтическим схемам.
После проведения противовоспалительного лечения и контрольной кольпоскопии пациенткам назначался Изопринозин по 1,0 г 3 раза в сутки в течение 10 дней. По основному заболеванию шейки матки 31й (41,9%) из обследованных женщин потребовалось комбинированное лечение с использованием радиоволновой терапии.
Эффективность монотерапии Изопринозином оценивалась по лабораторным исследованиям ПЦРдиагностики ВПЧинфекции через 1,52 месяца по окончанию терапии. Полученные результаты свидетельствуют, что полная элиминация вируса составила 95,3%, что подтверждено клиниколабораторным выздоровлением в 41 случае из 43х, что свидетельствует о высокой эффективности препарата.
При проведении комбинированной терапии с использованием радиоволновой методики воздействия на шейку матки и иммунокорригирующих препаратов эффективность лечения оценивалась через 2 месяца и полгода. Кольпоскопия показала, что у 30 (96,8%) обследуемых установлена нормальная кольпоскопическая картина, рецидив ВПЧинфекции имел место лишь в одном случае.
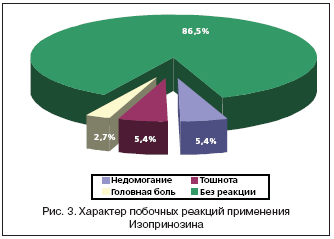
Кроме клинической эффективности, проведена оценка переносимости препарата Изопринозин. Установлено, что у 4 (5,4%) пациенток отмечалось легкое недомогание и тошнота, которые купировались на второй день приема препарата и не потребовали его отмены. Две пациентки жаловались на кратковременную головную боль, возможно, связанную с приемом препарата (рис. 3.). Других побочных проявлений и аллергических реакций не отмечено.
Таким образом, исследование, проведенное в группе подростков и молодых женщин с заболеваниями шейки матки на фоне папилломавирусной инфекции, и оценка эффективности изопринозина в монотерапии и комбинированном лечении позволяет сделать следующие выводы:
1. Большинство пациенток с папилломавирусной инфекцией имели отягощенный соматический и гинекологический анамнезы.
2. Папилломавирусная инфекция чаще сочетается с уреаплазмозом, микоплазмозом и кандидозом, которые в совокупности составили более 80% всех других возбудителей.
3. Изопринозин является высокоэффективным препаратом для лечения ВПЧинфекции при заболеваниях шейки матки у подростков и молодых женщин.
4. Эффективность в монотерапии Изопринозином составляет 95,3%. При использовании Изопринозина в сочетании с радиоволновой терапией эффективность достигает 96,8% при контроле через полгода, несмотря на выраженные первоначальные морфологические изменения шейки матки.
5. Учитывая высокую эффективность препарата, хорошую переносимость и отсутствие побочных явлений, Изопринозин может быть использован при лечении девочекподростков и юных женщин.
Литература
1. Голованова В.А. Гуркин Ю.А. Новик В.И. // Актуальные вопросы детской и подростковой гинекологии. материалы и тез. докл. Всерос. науч.практ. конф. Новосибирск, 1998. С. 148150.
2. Минкина Г.Н. Предрак шейки матки / Г.Н. Минкина, И.Б. Манухин, Г.А. Франк. М. 2001. С. 6972.
3. Прилепская В.Н. Генитальные инфекции и патология шейки матки. Клинические лекции / В.Н. Прилепская, Е.Б. Рудакова. Омск: ИПЦ ОмГМА, 2004. 212 с.
4. Прилепская В.Н. Заболевания шейки матки, влагалища и вульвы / В.Н. Прилепская. М. МЕД прессинформ, 2005. 432 с.
5. Прилепская В.Н. Вирус папилломы человека: современный взгляд на проблему / В.Н. Прилепская // Медицинский вестник. 2007. № 29 (414). С. 910.
6. Рудакова Е.Б. Псевдоэрозии шейки матки. автореф. дис. дра мед. наук / Е.Б. Рудакова. Омск, 1996. 34 с.
7. Роговская С.И. Оптимизация лечения хронических цервицитов с помощью изопринозина / С.И. Роговская, В.Н. Прилепская // Гинекология. 2006. Т. 8, № 1. С. 47.
8. Тихонова Л.И. Общий обзор ситуации с инфекциями, передаваемыми половым путем / Л.И. Тихонова // Вестн. дерматологии и венерологии. 1999. № 2. С. 47.
9. Auborn K.J. Treatment of human papillomavirus gynecologic infections / K.J. Auborn, T.H. Carter // Clin Lab Med. 2000. Vol. 20, N 2. P 407422.
10. Guidelines 2002 for treatment of sexually transmitted diseases / CDC Alanta. USA. 400 p. Workowski, K.A. Sexually Transmitted Diseases Treatment Guidelines 2002 / K.A. Workowski, W.C. Levine // MMWR Recomm Rep. 2002. Vol. 51 (RR6). P. 178.
11. Nagai Y. Persistence of human papillomavirus infection after therapeutic conization for CIN 3: is it an alarm for disease recurrence? / Y. Nagai, T. Maehama, T. Asato, K. Kanazawa // Gynecol Oncol. 2000. Vol. 79, N 2. P. 294299.
Источник: http://www.rmj.ru/articles_6084.htm
19.03.2015 | Админ | Просм. 53 | Комм. x | Категория: Выбор пользователей
